
薬づくりが変わる、業界が変わる。
このシリーズでは「製薬業界を変えるAI技術」と題して、創薬AIに関連する研究を毎週ご紹介します。以下のような用途でご活用ください。
- 業界の将来予測
- AI技術調査
- 各病における治療法の展望
担当するのは薬学部出身ライター、Masashiです。
今回は以下の5つの研究に注目していきます!
今週のラインナップ
1. 血液脳関門の透過性を予測
2. 標的タンパク質ごとにDTIを予測
3. 口腔がんの標的遺伝子を予測
4. 抗マラリア薬候補を予測
5. 希少疾患(ファンコニ貧血)の標的を予測
バックナンバーはこちら
血液脳関門の透過性を予測
中国・マカオ科学技術大学(2019年6月19日発表)
血液脳関門(BBB)は、中枢神経系(CNS)機能の維持に関わり、血液から脳組織への物質の移行を制限する役割を担っています。BBB透過性の有無がCNS薬の条件を満たす項目の一つであるため、BBB透過性の正確な予測が期待されています。
中国にあるマカオ科学技術大学の研究者らは、ディープラーニング手法を用いて、薬物の副作用や適応症例などの臨床データに基づいた血液脳関門の透過性予測モデルの開発を行いました。
結果、ディープラーニングが他の既存の機械学習モデルよりも優れたパフォーマンスを示し、平均精度は0.97に達しました。今後は、薬物がBBBにどのように透過するのかを予測するため、薬物の化学構造特性を組み合わせた予測モデルの構築が実施されるでしょう。
ソース:Improved Classification of Blood-Brain-Barrier Drugs Using Deep Learning.
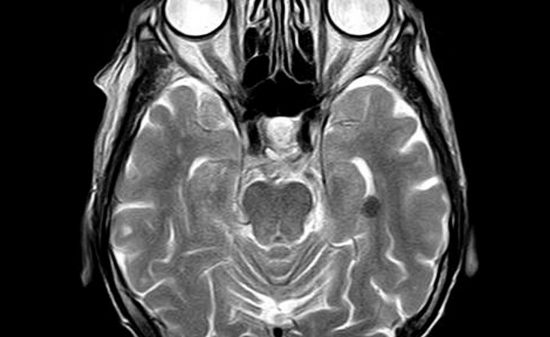
関連記事: 古典的な画像処理はMRIから脳腫瘍を発見できるか?
標的タンパク質ごとにDTIを予測
中国・安徽大学(2019年12月24日発表)

■サポートのお願い
AIDBを便利だと思っていただけた方に、任意の金額でサポートしていただけますと幸いです。





























 PAGE TOP
PAGE TOP